रोज़ाना हमें कोविड-19 के बारे में कुछ ना कुछ पता चलता रहता है: यह कितनी आसानी से लोगों को संक्रमित कर रहा है और व्यक्ति से व्यक्ति में फैल रहा है, और कैसे वैज्ञानिकों और चिकित्सा विशेषज्ञों ने इसके प्रसार के खिलाफ जंग छेड़ रखी है। हम यह भी सुनते हैं कि कैसे यह बैक्टीरिया से अलग है और क्यों एंटीबायोटिक दवाइयां इसका सफाया करने में कारगर नहीं हो सकतीं।
आखिर वायरस और बैक्टीरिया में अंतर क्या है? बैक्टीरिया सजीव होता है। हर बैक्टीरिया कोशिका में पुनर्जनन करने की प्रणाली होती है। यदि आप एक बैक्टीरिया कोशिका को लें और उसे पोषक तत्वों से युक्त घोल में डालें तो यह उसमें स्वयं वृद्धि कर सकता है, और विभाजित होकर अपनी संख्या वृद्धि कर सकता है। कोशिकाओं में मौजूद जीन (जीनोम, जो डीएनए अणुओं से बना होता है और जिसमें निहित जानकारी संदेशवाहक अणु आरएनए के लिए एक संदेश के रूप में लिखी होती है) में निहित संदेश प्रोटीन नामक कार्यकारी अणु में परिवर्तित हो जाता है जो बैक्टीरिया को पनपने और संख्या वृद्धि करने में मदद करता है। कोरोनावायरस में डीएनए नहीं होता लेकिन आरएनए होता है; दूसरे शब्दों में कहें तो वे केवल संदेश पढ़ सकते हैं, संदेश लिख नहीं सकते। इसलिए ये ‘मृतप्राय’ होते हैं जो स्वयं वृद्धि और पुनर्जनन नहीं कर सकते, इसके लिए उन्हें सहायता की दरकार होती है। यह सहायता वे ‘मेज़बान कोशिकाओं’ को संक्रमित करके लेते हैं और लाखों की संख्या में वृद्धि करते हैं। बिना सहायक मेज़बान कोशिका के वायरस एक बेकार वस्तु के समान है।
पॉलीप्रोटीन रणनीति
संक्रमण होने पर इस आरएनए की 33,000 क्षारों की शृंखला अमीनो अम्लों की एक लंबी शृंखला में तब्दील हो जाती है। चूंकि इस लंबी शृंखला में कई प्रोटीन होते हैं इसलिए इसे ‘पॉलीप्रोटीन’ अनुक्रम कहा जाता है। तो हमें इस पूरी पॉलीप्रोटीन शृंखला का विश्लेषण करना होता है, संक्रमण के लिए ज़िम्मेदार प्रोटीन पता करना होता है, उसे अलग करना होता है और संक्रमण में इन प्रोटीन की भूमिका पता करना होता है। (वैज्ञानिक पॉलीप्रोटीन को सिंगल रीडिंग फ्रेम कहते हैं जिसमें कई ओपन रीडिंग फ्रेम होते हैं। ये फ्रेम एक स्टार्ट कोड के साथ शुरु और एक स्टॉप कोड के साथ समाप्त होते हैं। और इनमें से प्रत्येक में वह प्रोटीन होता है जिसे मेज़बान कोशिका द्वारा व्यक्त किया जाना है)। यह युक्ति वायरल जीनोम को सघन रखती है और आवश्यकता पड़ने पर ही प्रोटीन व्यक्त करती है। यह कुछ हद तक उस किफायती व्यक्ति की तरह है जो बैंक में अपना पैसा फिक्स्ड डिपॉज़िट करके रखता है और वक्त पर ज़रूरत के हिसाब से पैसा निकालता है। वायरस की ज़रूरत मेज़बान को संक्रमित करके अपनी संख्या बढ़ाने की है। यदि कोई ज़रूरत नहीं, तो कुछ खर्च नहीं, तो कोई संक्रमण नहीं, और संख्या में वृद्धि नहीं!
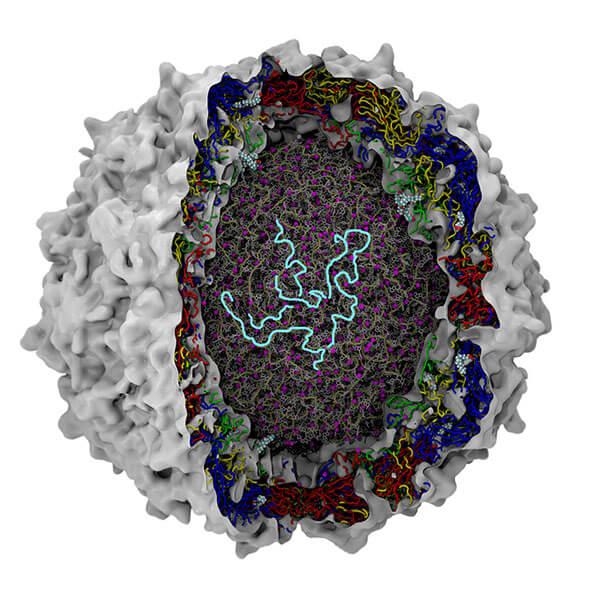
यू चेन और उनके साथी जर्नल ऑफ मेडिकल वायरोलॉजी में प्रकाशित अपनी हालिया समीक्षा में बताते हैं कि कोविड-19 की पॉलीप्रोटीन शृंखला में आरएनए-आधारित जीनोम और उप-जीनोम होते हैं, जो स्पाइक प्रोटीन (S), झिल्ली प्रोटीन (M), आवरण प्रोटीन (E) और न्यूक्लियोकैप्सिड प्रोटीन (N, जो वायरस की कोशिका के केन्द्रक की सामग्री का आवरण होता है) के लिए कोड करते हैं। ये सभी प्रोटीन वायरस के निर्माण के लिए आवश्यक होते हैं। इसके अलावा, खास संरचना के लिए ज़िम्मेदार प्रोटीन और अतिरिक्त सहायक प्रोटीन भी होते हैं जिन्हें गैर-निर्माणकारी प्रोटीन (NSP) कहा जाता है। इनमें से 16 प्रोटीन वायरस के संक्रमण और वृद्धि में मदद करते हैं।
इस तरह हमारे पास वायरस के प्रोटीन्स की एक खासी तादाद उपलब्ध है, जिनके निर्माण को बाधित करने या रोकने के लिए हम कई संभावित अणुओं और दवाइयों का परीक्षण कर सकते है। वास्तव में, पिछले महीने प्रकाशित हुए कई अध्ययनों में ऐसा ही करने की कोशिश की गई है।
इनमें से एक अध्ययन में वायरस के प्रमुख एंज़ाइम RDRp के निर्माण को लक्ष्य करने का प्रयास किया था, जिसका निर्माण रेमेडेसेविर दवा द्वारा रोका गया था। अमेरिका, जर्मनी और चीन के तीन अध्ययनों में वायरस के स्पाइक (S) प्रोटीन को बनाने वाले एंज़ाइम (जिसे 3CLpro या Mpro कहा जाता है) का निर्माण रोकने के तरीकों का विवरण है। और यू चेन ने उपरोक्त पेपर में वायरस के पॉलीप्रोटीन के 16 से अधिक गैर-निर्माणकारी प्रोटीन (NSP) सूचीबद्ध किए हैं, जिनका निर्माण संभावित दवाइयों द्वारा रोका जा सकता है। (बोस्टन के डॉ. पांडुरंगाराव का मत है कि इनमें से भी एंज़ाइम NSP12 एक महत्वपूर्ण व लाभदायक लक्ष्य होगा)।
इस संदर्भ में यहां भारतीय शोधकर्ता तनीगैमलाई पिल्लैयार के काम का उल्लेख महत्वपूर्ण होगा। पिल्लैयार 2013 से जर्मनी स्थित युनिवर्सिटी ऑफ बॉन में औषधी रसायनज्ञ के रूप में कार्यरत हैं। साल 2016 में जर्नल ऑफ मेडिसिनल केमिस्ट्री में प्रकाशित शोध पत्र में उन्होंने SARS-CoV के मुख्य एंज़ाइम कीमोट्रिप्सीन-नुमा सिस्टीन प्रोटीएज़ (3CLpro या Mpro) की 3-डी मॉडलिंग करके सम्बंधित वायरस TGEV (ट्रांसमिसेबल गैस्ट्रोएंटेराइटिस वायरस) का पता लगाया और उसके एक्स-रे क्रिस्टल संरचना की मदद से उन्होंने पता लगाया कि यह एंज़ाइम वायरस की संरचना में ताला-चाभी तरीके से जुड़ता है। इस आणविक मॉडलिंग के बाद उन्होंने ऐसी दवा की पड़ताल की जो इस बंधन को निष्क्रिय कर सके और SARS-CoV को संक्रमित करने से रोक सके। अनुमान था कि लगभग 160 ज्ञात दवाएं यह कार्य करने में विभिन्न दक्षता के साथ कारगर हो सकती हैं। दवाओं की यह सूची क्रिस्टल संरचना की जानकारी के 3-4 साल पहले सुझाई गई थी, जिसे पिल्लैयार और उनके साथियों ने जनवरी 2020 में ड्रग डिस्कवरी टुडे में प्रकाशित, अपने हालिया शोध पत्र में अपडेट किया है।
भारत को पिछले 90 वर्षों से कार्बनिक और औषधीय रसायन के क्षेत्र में खासा अनुभव हासिल है। भारत गुणवत्तापूर्ण औषधि निर्माण, और 1970 पेटेंट अधिनियम के बाद से निर्यात में कुशलता पूर्वक कार्य कर रहा है। आज हमारी दक्षता सार्वजनिक और निजी दोनों क्षेत्रों में न केवल ज़रूरत के मुताबिक अणुओं को संश्लेषित करने की है बल्कि कंप्यूटर मॉडलिंग की मदद से बैक्टीरिया और वायरस के प्रोटीन को लक्ष्य करने में, होमोलॉजी मॉडलिंग, ड्रग डिज़ाइन, दवाओं के नए उपयोग खोजने वगैरह में भी है।
CSIR ने इस जानलेवा वायरस का मुकाबला करने वाले रसायन और तरीकों को विकसित करने की ज़िम्मेदारी ली है, और हमें पूरी उम्मीद है कि वे निकट भविष्य में अवश्य सफल होंगे! (स्रोत फीचर्स)
नोट: स्रोत में छपे लेखों के विचार लेखकों के हैं। एकलव्य का इनसे सहमत होना आवश्यक नहीं है।
Photo Credit : https://www.thehindu.com/sci-tech/science/xaced1/article31375821.ece/ALTERNATES/FREE_960/19TH-SCICORONAVIRUS